Teori Atom Dalton
Pada tahun 1803, seorang ilmuwan berkebangsaan Inggris bernama John Dalton mengemukakan teori atom berdasarkan hukum kekekalan massa dan hukum perbandingan tetap. John Dalton merumuskan tiga asumsi pokok, yaitu:

- Unsur kimia tersusun oleh partikel-partikel kecil yang tidak dapat dihancukan dan dipisahkan yang disebut atom
- Setiap atom dari suatu unsur memiliki massa dan sifat yang sama, namun berbeda dengan unsur lainnya
- Dua atom atau lebih membentuk senyawa dengan perbandingan tetap dan tertentu
Teori Atom Thomson
Pada tahun 1897, Joseph John Thomson melalkukan eksperimen dengan tabung sinar katode dan menemukan bahwa sinar katode adalah berkas partikel bermuatan negatif yang disebut dengan elektron yang ada pada setiap materi. Model atom Thomson dianalogikan seperti sebuah roti kismis, dimana atom terdiri atas materi bermuatan positif dan di dalamnya tersebar elektron bagaikan kismis yang terdapat dalam roti kismis. Muatan positif dan negatif dalam atom memiliki jumlah yang sama maka secara keseluruhan, atom menurut Thomson bersifat netral

Teori Atom Rutherford
Pada tahun 1911, Ernest Rutherford dengan bantuan muridnya Hans Geiger dan Ernest Marsden melanjutkan eksperimen Lenard yang menyatakan bahwa elektron tersebar merata dalam muatan positif atom adalah tidak benar. Rutherford melakukan percobaan penembakan sinar alfa pada lempeng emas. Ernest Rutherford mengungkapkan teori atom sebagai berikut:
- Atom tersusun atas elektron-elektron yang bermuatan negatif yang mengelilingi inti
- Semua proton terkumpul dalam inti atom dan menyebabkan inti atom bermuatan positif
- Sebagian besar ruang dalam atom adalah ruang hampa
- Jumlah proton dalam inti sama dengan jumlah elektron yang mengelilingi inti sehingga atom bersifat netral

Teori Atom Bohr
Pada tahun 1913, seorang ilmuwan dari Denmark yang bernama Niels Henrik David Bohr menyempurnakan model atom Rutherford. Dengan teori mekanika kuantum Planck, Bohr menyampaikan 2 postulat yang menjelaskan kestabilan atom, yaitu:
- Elektron mengelilingi inti atom pada lintasan tertentu yang stasioner yang disebut orbit/kulit sehingga elektron tidak jatuh ke inti
- Elektron dapat berpindah dari kulit yang satu ke kulit yang lain dengan memancarkan atau menyerap energi yang disebut dengan energi foton

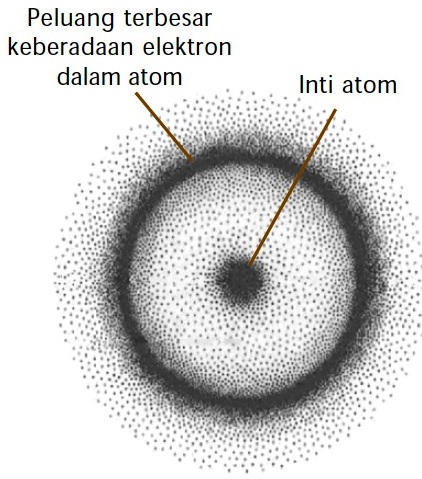
Teori Atom Mekanika Kuantum
Teori atom mekanka kuantum didasarkan pernyataan tiga ilmuwan, yaitu:
- Louis de Broglie, menyatakan bahwa atom mempunyai sifat dualisme, yaitu sebagai partikel dan sebagai gelombang
- Werner Heisenberg, menyatakan bahwa terdapat asas ketidakpastian dimana tidak mungkin menentukan posisi dan momentum elektron yang pasti dalam atom
- Erwin Schrodinger, menyatakan bahwa volume ruang yang memiliki kebolehjadian terbesar untuk menentukan elektron disebut dengan orbital atom.